ALZHEIMER FAMILIAR
Un equipo argentino desarrolló neuronas humanas a partir de células de un paciente con Alzheimer familiar. El modelo permite estudiar mecanismos celulares de la enfermedad con mayor precisión y abre nuevas perspectivas para comprender procesos que no pueden observarse directamente en el cerebro humano.
El principal logro del trabajo fue la generación de neuronas humanas a partir de células de la piel de un paciente con enfermedad de Alzheimer familiar (EAF). Este avance permitió desarrollar un modelo experimental que reproduce, en condiciones de laboratorio, características propias de la patología en un contexto biológico más cercano al humano.
La investigación se enfocó en una mutación específica, la M146L en la proteína Presenilina-1, identificada en una familia argentina con antecedentes de Alzheimer hereditario. Este tipo de Alzheimer, aunque representa menos del 1% de los casos, resulta especialmente valioso para la investigación porque existe una relación directa entre la alteración genética y la enfermedad, lo que facilita el estudio de los mecanismos implicados.
En qué consiste el modelo y sus resultados
El modelo desarrollado se basa en el uso de células madre pluripotentes inducidas (iPSC). Estas células se obtienen a partir de células adultas -en este caso, de la piel del paciente- que son reprogramadas para volver a un estado indiferenciado, con la capacidad de transformarse en distintos tipos celulares.
A partir de este proceso, los investigadores lograron generar neuronas humanas portadoras de la mutación asociada al Alzheimer familiar. Esto permitió observar, en condiciones controladas, cómo se comportan estas células y qué alteraciones presentan en comparación con neuronas sin la mutación.
Una de las ventajas centrales de este enfoque es que permite estudiar la enfermedad en células humanas reales, evitando las limitaciones de los modelos animales o de líneas celulares artificiales, que no siempre reflejan con precisión lo que ocurre en el cerebro humano.
Dado que no es posible trabajar directamente con neuronas del cerebro de los pacientes, los investigadores utilizaron un procedimiento ampliamente desarrollado en biología celular, la reprogramación celular.
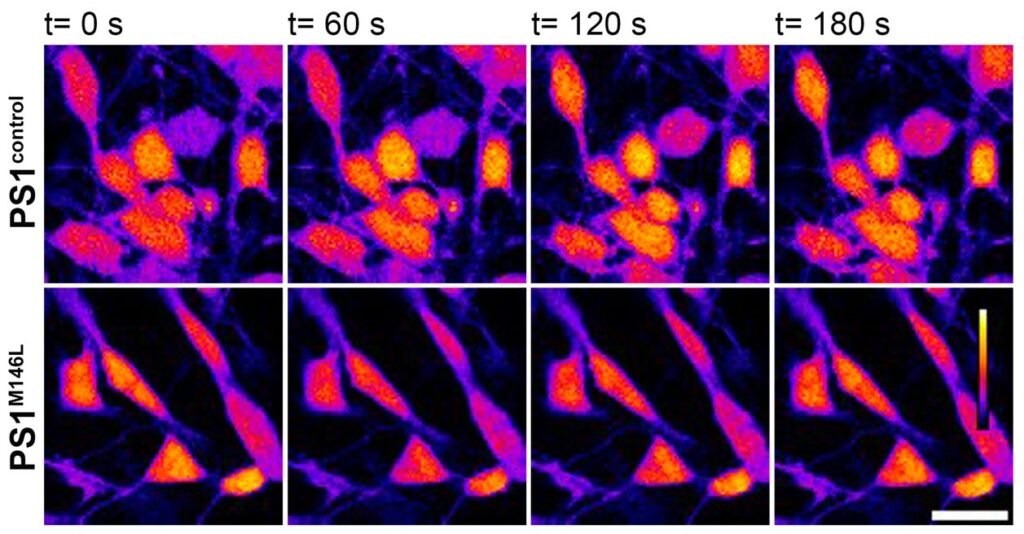
Los resultados mostraron que las neuronas portadoras de la mutación presentan alteraciones en la dinámica del calcio y un funcionamiento defectuoso de las mitocondrias, estructuras responsables de la producción de energía en la célula.
Estos cambios se asocian con un aumento en la producción de especies reactivas de oxígeno y con la activación de procesos inflamatorios, factores que contribuyen a la neurodegeneración.
Este hallazgo es relevante porque amplía la mirada tradicional sobre el Alzheimer, históricamente centrada en la acumulación de la proteína beta-amiloide. Si bien este proceso sigue siendo importante, el estudio sugiere que existen otros mecanismos celulares que también desempeñan un rol clave.
El modelo desarrollado es especialmente útil para el estudio del Alzheimer familiar, ya que reproduce una mutación genética específica y sus efectos en las neuronas. En cambio, el Alzheimer esporádico -que representa la gran mayoría de los casos- es una enfermedad multifactorial, en la que intervienen múltiples variables genéticas, ambientales y de estilo de vida.
Un avance con proyección
El desarrollo de neuronas humanas a partir de células de pacientes representa un paso significativo en la investigación de enfermedades neurodegenerativas. Este tipo de modelos permite estudiar procesos celulares con un nivel de detalle que antes no era posible, abriendo nuevas líneas de investigación.
El estudio fue coordinado por Alfredo Cáceres, Laura Morelli y Luis Ignacio Brusco, quienes lideraron el diseño y la interpretación de los resultados. Laura Morelli aportó la perspectiva desde el Laboratorio de Envejecimiento Cerebral y Neurodegeneración, destacando la relevancia del modelo humano y su capacidad para reproducir la fisiología neuronal. Alfredo Cáceres, desde el CIMETSA, contribuyó al análisis de los mecanismos celulares y al enfoque sobre la relación causa-efecto en el Alzheimer familiar, mientras que Luis Ignacio Brusco sumó la mirada clínica, vinculando los hallazgos con su impacto en la comprensión de la enfermedad en humanos.
El trabajo contó además con la participación de Carlos Wilson, primer autor, quien llevó adelante los experimentos y el análisis del estado metabólico neuronal. También participaron Eduardo Castaño, Pablo Galeano, Gisela Novack, Lorenzo Campanelli, Andrés H. Rossi y Esteban Miglietta, desde la Fundación Instituto Leloir, en el desarrollo experimental y análisis de datos; María Mónica Remedi y Laura Gastaldi, desde el CIMETSA, en la generación y caracterización del modelo celular; y Natividad Olivar, desde la Facultad de Medicina de la UBA, con aportes en el plano académico y clínico.
Foto: Imágenes representativas de la captación de calcio en las neuronas “control” (arr.) y en aquellas que presentan la mutación PS1 M146L (abajo) en el tiempo: de 0 a 180 segundos. Fundación Instituto Leloir.